Вступ
Переробка відпрацьованих каталізаторів — актуальна проблема сучасної хімічної інженерії. В азотній промисловості (виробництво нітратів і нітратної кислоти) застосовують як металічні (платинові ґрати, сплави Pt–Rh), так і підтримувані каталізатори з активними металами, нанесеними на оксидні носії (Al₂O₃, SiO₂, TiO₂). Відпрацьовані каталізатори містять цінні метали та носій, що вимагає розробки технологічних схем їхньої комплексної переробки з метою видобутку цінних компонентів та регенерації носія для повторного використання. Типовими об’єктами є платинові та платинородієві ґрати та підтримувані каталізатори із оксидами металів на Al₂O₃/SiO₂. Основні проблеми: забруднення продуктами зношування, спікання носія, хімічне забруднення (сульфати, хлориди, карбонати), агрегація частинок та втрати поверхні, що призводить до зниження каталізаторної активності [1, c. 459].
Методи переробки відпрацьованих каталізаторів азотної промисловості
У таблиці 1 наведено опис сучасних підходів до видалення активної фази з відпрацьованих каталізаторів і регенерації оксидних носіїв.
Таблиця 1
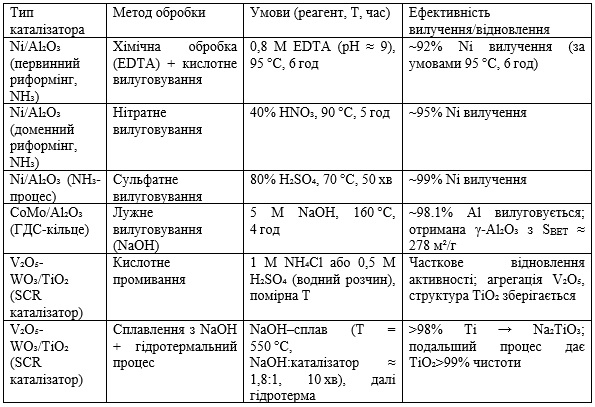
Характеристика сучасних методів регенерації оксидного носія різних типів каталізаторів
Видалення активної фази із каталізаторів зазвичай здійснюють за допомогою гідрометалургійних методів: кислотного вилуговування або хелатування. Сульфатне розчинення в H₂SO₄ при високій концентрації показало максимальну ефективність. Так, робота [2, c. 52] повідомляє про 99% вилучення Ni з використаного каталізатора NH₃-процесу (Ni/Al₂O₃) при 70 °C за 50 хв. Подібні результати продемонстровано у [3, c. 26]: 95% вилуговування Ni при 90 °C за 5 год у 40% розчині HNO₃. Використання хелатних агентів (EDTA) також ефективне: в роботі [4, c. 8] досягнуто вилуговування 92% Ni з аналогічного Ni/Al₂O₃ каталізатора при 95 °C за 6 год з 0,8 М EDTA.
Регенерація оксидного носія зазвичай потребує додаткової обробки після вилуговування. За даними [5, c. 40], обробка CoMo/Al₂O₃ у лужному середовищі (5 М NaOH, 160 °C, 4 год) вилуговує ~98% Al, залишаючи у залишку збагачені Ni і Co. З екстрагованого розчину готують γ-Al₂O₃ з високою питомою площею (~278 м²/г). Отже, лужне вилуговування дозволяє ефективно відновити каркас носія у вигляді дрібнодисперсного γ-Al₂O.
Для каталітичних структур на основі TiO₂ (типу V₂O₅–WO₃/TiO₂ у SCR) запропоновані як гідрометодики, так і комбіновані хіміко-термічні підходи. В роботі [6, c. 3092] показано, що промивка відпрацьованого SCR-каталізатора водними розчинами амоній хлориду (1 М NH₄Cl) або розведеної сульфатної кислоти (0,5 М H₂SO₄) частково відновлює активність; при цьому агрегація V₂O₅ розпадається, а структура TiO₂ (анатаз) залишається стабільною. В альтернативному підході [7, c. 142767] запропонували «молекулярний» метод: сплавлення із NaOH при 550 °C утворює α-Na₂TiO₃ (>98% конверсія Ti), а наступна гідротермальна обробка дає високочистий TiO₂ (>99% чистоти). Такий процес дозволяє повністю перетворити титан у функціональний TiO₂, придатний для фотокаталізу.
Таким чином, огляд літератури свідчить, що кислотне вилуговування є ефективним для вилучення металів (Ni, Mo, Co тощо) з носієм Al₂O₃/SiO₂. Лужне вилуговування (наприклад, NaOH) дає змогу звільнити та зберегти каркас носія. Хелатні агенти (EDTA, тощо) також успішно застосовуються, але потребують більш тривалого часу та буфера pH. Для TiO₂-носіїв показові методи включають іонний обмін (NH₄Cl) та нітратну/сульфатну кислоту (для видалення V, W), а також комбінацію термічної сплавки з лугом і гідротермії для повного відновлення TiO₂. Кожен метод забезпечує певний рівень відновлення поверхні носія (питома площа, пористість) і розподілу фаз, що характеризують регенерований матеріал. Зокрема, отримані регенеровані носії часто демонструють великий питомий об’єм (γ-Al₂O₃ ≈ 278 м²/г) та дрібні кристаліти (розмір зерен < 25 нм), які є сприятливими для каталізатора.
Різні підходи до регенерації мають свої переваги: кислотне вилуговування є відносно простим і високоефективним для видалення металів, тоді як лужне вилуговування дає змогу накопичити носій у формі розчинних гідрокомплексів і відновити його у вигляді чистого оксиду. Комбіновані методи (хімічна обробка + термічна або гідротермальна обробка) дозволяють гнучко варіювати кінцеві властивості регенерованих оксидів. В цілому, сучасні дослідження демонструють, що при грамотному виборі реагентів та умов можна ефективно повернути цінні компоненти з відпрацьованих каталізаторів та забезпечити високу якість регенерованого носія.
Пропонована технологічна схема комплексної переробки є наступною:
1. Підготовка і механічна очистка — розбір ґрат/каркасів, подрібнення, сортування за фракціями; видалення нафтопродуктів і органічних забруднень шляхом промивки органічними розчинниками або термічного піролізу.
2. Термічна обробка (проміжна) — окиснювальний спал (400–600 °C) для видалення органіки та переводу металевого стану домішок у більш доступні форми. Метою є також розпушення спечених частинок носія.
3. Хімічне вилуговування активної фази — застосування гідрометалургійних розчинів (розведені кислоти: HCl, H₂SO₄ або комплексоутворювальні розчини: амоніачні, тіосульфатні, сульфітні системи) для вилучення розчинних форм металів (Cu, Ni, V, платина тощо). Параметри: T, pH, час контакту й співвідношення твердого/рідкого підбираються для селективності.
4. Нейтралізація та промивка — приведення залишкових розчинів до безпечного рівня, багаторазова промивка носія водою для видалення іонних домішок.
5. Стабілізація та регенерація носія — відновлювальна обробка (наприклад, термообробка при 500–800 °C для відновлення пористої структури Al₂O₃ чи TiO₂), корекція текстури за допомогою промивки, внесення оксидних доповнень (карбонатні або алюмінієві добавки) при необхідності.
6. Контроль якості регенерованого носія — визначення питомої площі (метод БЕТ), пористості, механічної міцності, хімічного складу (SEM–EDS, XRD).
7. Повторне нанесення активної фази (опціонально) — імпрегнація носія солями платини/інших металів та подальша активація (сушка, прожарювання, відновлення).
Для оцінки ефективності регенерації слід використовувати: хімічний аналіз (атомно-абсорбційна спектрометрія або ICP-OES) для визначення вмісту металів; пористість і питома площа (БЕТ); рентгенівська дифракція (XRD) для фазового складу; скануюча електронна мікроскопія (SEM) — для морфології; механічні випробування на міцність гранул/сфер. На основі цих даних порівнюють регенерований носій із вихідним.
Реалізована комплексна схема повинна забезпечити: значне вилучення цінних металів у розчинні концентрати (далі — для повернення у виробництво або продажу); збереження/відновлення не менше 60–80 % питомої поверхні носія залежно від ступеня пошкодження; зниження обсягу відходів, що підлягають захороненню. Найскладнішим етапом є селективне вилучення активних металів при мінімальних втрати носія — це вимагає оптимізації pH і вибору комплексоутворювальних реагентів.
Переваги схеми: зменшення споживання первинних оксидів (економія ресурсів), зниження викидів та обсягів токсичних відходів. Необхідні витрати пов’язані з обладнанням, обробкою розчинів і енергоємними стадіями. За попередніми розрахунками для підприємств азотної промисловості окупність інвестицій у схему можлива за умови високого вмісту металів у відходах та налагодженого ринку вторинної сировини.
Висновки
1. Розроблена технологічна схема поєднує механічну, термічну та гідрометалургійну обробки й дозволяє отримати регенерований оксидний носій, придатний для повторного використання.
2. Ключовими параметрами є вибір реагентів для вилуговування, умови термообробки та методи очищення носія.
3. Схема сприяє зменшенню впливу азотної промисловості на навколишнє середовище й підвищенню матеріальної ефективності, але потребує індивідуальної оптимізації для конкретних типів каталізаторів (платинові ґрати, підтримувані системи).
Список літератури
1. Panggabean T. K. M. A. et al. Utilization of the spent catalyst as a raw material for rechargeable battery production: The effect of leaching time, type, and concentration of organic acids. International Journal of Renewable Energy Development. 2023. Vol. 12. №. 3. P. 459.
2. Oza R., Shah N., Patel S. Nickel Recovery from Spent Ni/Al O Catalysts Using Nitric Acid Solution. Asian Journal of Water, Environment and Pollution. 2011. Vol. 8. №. 3. P. 51-58.
3. Singh B. Treatment of spent catalyst from the nitrogenous fertilizer industry—A review of the available methods of regeneration, recovery and disposal. Journal of Hazardous Materials. 2009. Vol. 167. №. 1-3. P. 24-37.
4. Liu Q. et al. Recovery and regeneration of Al2O3 with a high specific surface area from spent hydrodesulfurization catalyst CoMo/Al2O3. Rare Metals. 2019. Vol. 38. №. 1. P. 1-13.
5. Shang X. et al. Effective regeneration of thermally deactivated commercial VW-Ti catalysts. Frontiers of Chemical Science and Engineering. 2012. Vol. 6. №. 1. P. 38-46.
6. Zhang Q., Wu Y., Zuo T. Green recovery of titanium and effective regeneration of TiO2 photocatalysts from spent selective catalytic reduction catalysts. ACS Sustainable Chemistry & Engineering. 2018. Vol. 6. №. 3. P. 3091-3101.
7. Wen C. et al. Disposal of spent V2O5-WO3/TiO2 catalysts: A regeneration principle based on structure-activity relationships from carrier transformations. Chemosphere. 2024. Vol. 363. P. 142767.
|