Стійкий комплекс порушень метаболізму вуглеводів за адипозитозу призводить до клінічного стану відомого як “цукровий діабет ІІ типу” або метаболічного синдрому. Згідно даних Всесвітньої організації охорони здоров’я, у 2022 році (останнє оновлення даних) 14% дорослих у віці 18 років і старше страждали на цукровий діабет. Це на 7% більше порівняно із 1990 роком. Більше 95% випадків цукрового діабету припадає на цукровий діабет 2-го типу. Враховуючи тенденцію до поширення захворювання, у травні 2021 року Всесвітня асамблея охорони здоров’я прийняла резолюцію щодо посилення профілактики та контролю цукрового діабету [1]. Тобто за узагальненою статистикою, від цього стану страждають кожні дві людини з десяти - при цьому майже у 50% тих хто страждає на гіперглікемію мають ожиріння, яке і зумовило подальше порушення вуглеводного метаболізму.
Однією з початкових ланок патоморфологічних процесів за метаболічного синдрому є клітинна дисфункція ендотеліоцитів кишківника, що призводить до порушення кишкового бар’єру та міграції бактеріальних ліпополісахаридів до печінки з подальшим запальним процесом, який стає каскадним через розвинену жирову тканину, яка відіграє ключову роль у вивельнені цитокінів, беручи участь у секреції адипонектину, лептину, TNF и IL-6. Крім того, деякі ліпідні речовини, що вивільняються із адипоцитів (пальмітинова кислота, церамід), порушують функції ендоплазматичного ретикулума й мітохондрій, викликаючи загибель гепатоцитів внаслідок клітинного стресу [2].
Роль ендотеліальних клітин у розвитку метаболічного синдрому показова у механізмі розвитку алкогольної хвороби печінки. Алкоголь знижує експресію антимікробного білка REG3G у кишківнику, що призводить до збільшення кількості бактерій на слизовій оболонці кишок, порушення кишкового бар’єру, підвищення проникності кишківника й викликає ектопічну імунну стимуляцію - що у свою чергу є однією з причин розвитку метаболічного синдрому [3-4].
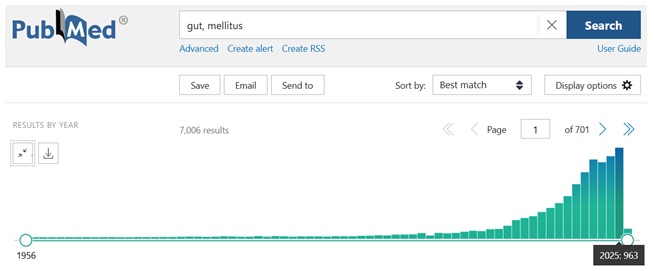
За останні 5 років збільшена кількість публікацій на порталі PubMed за ключевими словами “intestinal barrier, gut, mellitus” демонструє стабільний інтерес наукової спільности до ролі кишкового бар’єру у структурно-функціональних порушеннях організму (Рис.1).
Рис.1. Кількість публікацій за останні 5 років.
Враховуючи результати наших попередніх культуральних досліджень, що продемонстрували про-проліферативну активність триметилгліцину відносно ендотеліальних клітин аорти свині, а також загальну світову тенденцію на вивчення ролі кишкового бар’єру, ми вважаємо доцільним подальші дослідження у цьому напрямку.
Список літератури:
1. Diabetes. https://www.who.int/news-room/fact-sheets/detail/diabetes
2. Agnieszka Karkucinska-Wieckowska et al. (2022). Mitochondria, oxidative stress and nonalcoholic fatty liver disease: A complex relationship. Eur J Clin Invest, 52(3):e13622. DOI:10.1111/eci.13622
3. Hussen N et other. (2018). Hepatoptosis in a Patient with Alcoholic Hepatitis. Am J Gastroenterol. 2018 Nov;113(11):1581. DOI: 10.1038/s41395-018-0182-9
4. Weiskirchen R et other (2018). Recent advances in understanding liver fibrosis: bridging basic science and individualized treatment concepts. DOI: 10.12688/f1000research.14841.1
|