Актуальність. Рак яєчників залишається однією з провідних причин смертності серед злоякісних новоутворень жіночої репродуктивної системи, що зумовлено пізньою діагностикою та вираженою морфологічною і молекулярною гетерогенністю пухлин [1,2]. Традиційне гістологічне дослідження не завжди дозволяє точно визначити гістогенез і підтип пухлини, що може ускладнювати вибір оптимальної лікувальної тактики. У зв’язку з цим імуногістохімічне дослідження набуває особливої актуальності як інструмент уточнення діагнозу та молекулярної стратифікації пацієнток із раком яєчників [3,4].
Мета роботи. Оцінити роль імуногістохімічного дослідження у діагностиці раку яєчників шляхом аналізу експресії маркерів WT-1, p53, прогестеронового рецептора (PR) та Napsin A.
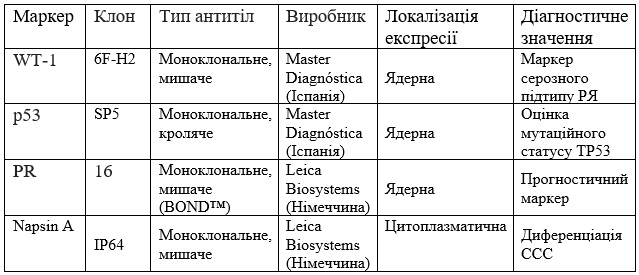
Матеріали та методи. Дослідження проведено на зразках пухлинної тканини пацієнток із епітеліальним раком яєчників, отриманих під час діагностичної лапароскопії або хірургічного лікування. Імуногістохімічне фарбування виконували на парафінових зрізах із застосуванням моноклональних антитіл до WT-1, p53, PR та Napsin A з використанням полімерної системи детекції та DAB-хромогену. Для даного дослідження було використано первинну панель моноклональних антитіл, адаптовану до гістологічних підтипів раку яєчників
( таб 1.).
Таблиця 1
Первинні антитіла, використані для імуногістохімічного дослідження
Оцінку експресії маркерів здійснювали методом світлової мікроскопії з урахуванням локалізації та характеру забарвлення пухлинних клітин. Оцінку імуногістохімічних реакцій проводили напівкількісним методом у не менше ніж 10 полях зору мікроскопа в тому числі при збільшенні х400. Позитивною реакцією вважали наявність коричневого забарвлення у пухлинних клітин з вираженою або помірно вираженою специфічною реакцією для кожного маркера.
Експресію p53 оцінювали за характером ядерного забарвлення та класифікували як патологічну (дифузне інтенсивне забарвлення >80% пухлинних клітин або повна відсутність експресії) чи «дикий тип» (гетерогенне ядерне забарвлення) [5]. Експресію PR визначали за наявністю ядерного забарвлення та вважали позитивною за умови експресії у ≥1% пухлинних клітин [6]. Позитивною експресією WT-1 вважали чітке ядерне забарвлення пухлинних клітин. Експресію Napsin A оцінювали за наявністю цитоплазматичного забарвлення та реєстрували як позитивну або негативну [7].
Діагноз встановлювали два незалежних досвідчених морфологи, які проводили аналіз відповідно до сучасних класифікацій ВООЗ [8,9].
Результати. Імуногістохімічне дослідження дозволило чітко диференціювати основні гістологічні підтипи епітеліального раку яєчників. Експресія WT-1 та патологічний тип експресії p53 переважали у серозних карциномах, тоді як позитивна експресія Napsin A була характерною для світлоклітинного раку яєчників. Визначення експресії PR виявило прогностичну значущість та потенційну роль у стратифікації пацієнток [10].
Висновки. Імуногістохімічне дослідження є важливим компонентом сучасної діагностики раку яєчників, що підвищує точність морфологічної верифікації, забезпечує диференційну діагностику гістологічних підтипів та сприяє персоналізованому підходу до лікування пацієнток.
СПИСОК ВИКОРИСТАНОЇ ЛІТЕРАТУРИ
1. González-Martín A, Harter P, Leary A, et al. Newly diagnosed and relapsed epithelial ovarian cancer: ESMO Clinical Practice Guideline for diagnosis, treatment and follow-up. Ann Oncol. 2023;34(10):833-848. doi:10.1016/j.annonc.2023.07.011
2. Kossaï M, Leary A, Scoazec JY, Genestie C. Ovarian cancer: a heterogeneous disease. Pathobiology. 2020;87(1):41–49. doi:10.1159/000502978.
3. Gupta S, Ahuja S, Kalwaniya DS. Immunohistochemistry Markers in Ovarian and Fallopian Tube Neoplasms: a Comprehensive Review. Indian J Surg Oncol. 2024;15(Suppl 3):465-480. doi:10.1007/s13193-024-02049-y
4. Ghuman M., Singh S. Immunohistochemical spectrum of ovarian neoplasms. Journal of Diagnostic and Academic Pathology. 2024. Vol. 10(1). P. 1–11.
doi: 10.4103/jdap.jdap_4_24
5. Chui, M.H.; Momeni Boroujeni, A.; Mandelker, D., et al. Characterization of TP53-wildtype tubo-ovarian high-grade serous carcinomas: Rare exceptions to the binary classification of ovarian serous carcinoma. Mod. Pathol. 2021, 34, 490–501. https://doi.org/10.1038/s41379-020-00648-y
6. Borella F., Fucina S., Mangherini L., et al. Hormone receptors and epithelial ovarian cancer: recent advances in biology and treatment options. Biomedicines. 2023. Vol. 11, № 8. P. 2157. doi: https://doi.org/10.3390/biomedicines11082157
7. Dewi I.G.A.S.M., Winata I.G.S. The role of Napsin A in differentiating clear cell type ovarian carcinoma from other high-grade ovarian carcinomas. Bali Medical Journal. 2025. Vol. 14, No. 1, P. 447–453. doi:10.15562/bmj.v14i1.5597
8. Colombo N, Sessa C, du Bois A, et al. ESMO-ESGO consensus conference recommendations on ovarian cancer: pathology and molecular biology, early and advanced stages, borderline tumours and recurrent disease†. Ann Oncol. 2019;30(5):672-705. doi:10.1093/annonc/mdz062
9. Höhn AK, Brambs CE, Hiller GGR, et al. 2020 WHO Classification of Female Genital Tumors. Geburtshilfe Frauenheilkd. 2021;81(10):1145-1153. doi:10.1055/a-1545-4279
10. Ittner, E., Swenson, H., Werner, L. et al. Diagnostic and prognostic biomarkers associated with histotype in advanced epithelial ovarian cancer. Sci Rep 15, 37171 (2025). https://doi.org/10.1038/s41598-025-24938-0
|